6. Reaktionsmechanismen¶
Die Synthese von Wasser könnte über verschiedene Wege ablaufen.
Beispielsweise könnten im Verlauf der Reaktion zuerst alle Bindungen gespalten werden, und dann alle neuen Bindungen wieder zusammengesetzt (Abb 1, Mechanismus 1).
Die Reaktion könnte aber auch schrittweise ablaufen, so dass zu keinem Zeitpunkt alle Bindungen gespalten sind. Bei Mechanismus 2 wird zunächst nur eine HH-Bindung gespalten und dann die Doppelbindung im Sauerstoffmolekül zu einer Einfachbindung. Dann beginnen sich bereits neue Bindungen auszubilden (Mechanismus 2). Mechanismus 3 beginnt hingegen mit der Spaltung der Doppelbindung zwischen den O-Atomen.
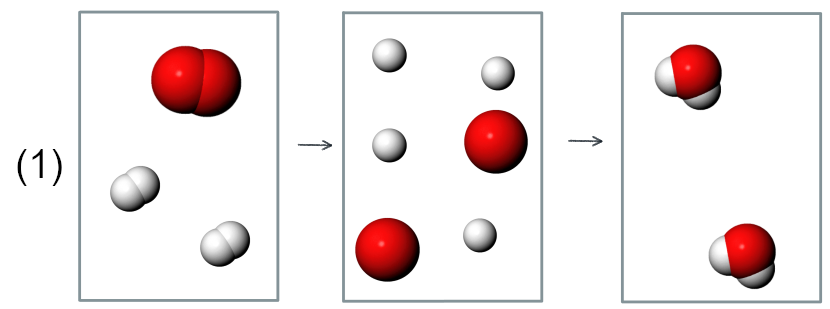
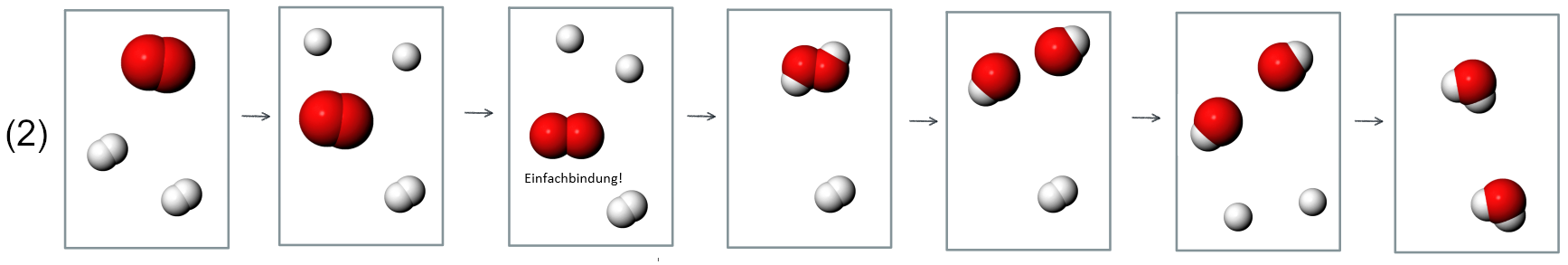
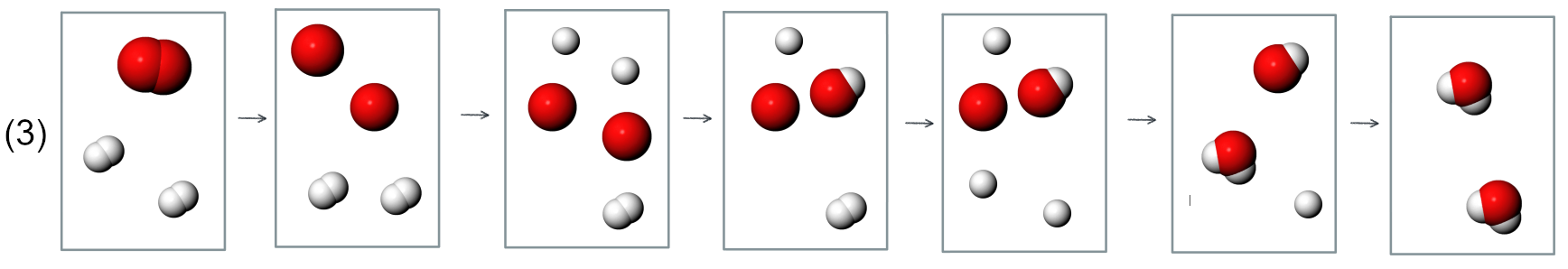
Abb 1: Mechanismen 1, 2 und 3¶
Folgende Abbildung zeigt den energetischen Verlauf der Reaktion, wie er sich aus den Bindungsenergien ergibt.
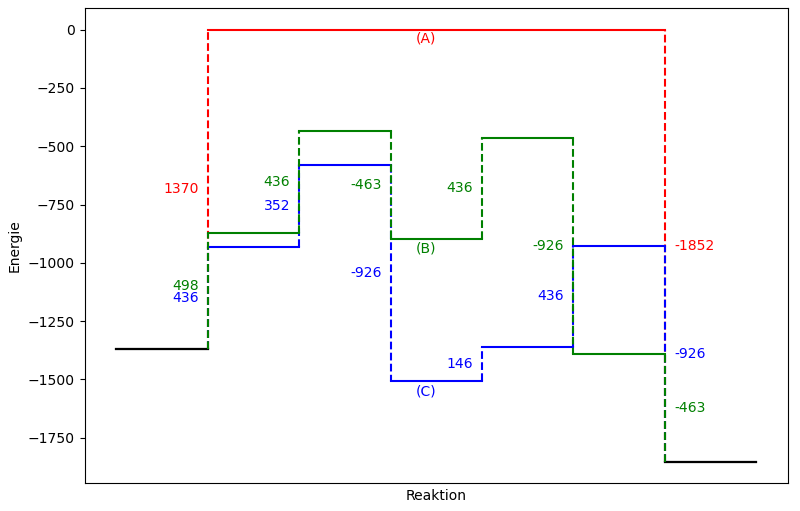
Abb 2: Mögliche Reaktionsverläufe der Synthese von Wasser.¶
Welcher Energetische Verlauf entspricht welcher der obigen Reaktionsmechanismen?
| Mechanismus 1 entspricht | |
| Mechanismus 2 entspricht | |
| Mechanismus 3 entspricht |
Die Edukte würden sehr unterschiedlich schnell über diese verschiedenen Mechanismen reagieren:
| Welcher dieser Mechanismen würde deutlich langsamer ablaufen als die anderen zwei? | |
| Welche Aussage trifft am besten zu? Die Reaktion verläuft vorwiegend |
Viele Reaktionen starten alleredings gar nicht damit, dass einzelne Bindungen ganz gebrochen werden. Stattdessen werden Bindungen oftmals immer schwächer, während bereits neue Bindungen geknüpft werden:
Was bedeutet diese gleichzeitige Ausbildung und Lockerung von Bindungen für die Aktivierungsenergie?
In anderen Fällen wird die Abspaltung eines Molekülteils begünstigt, indem sich das verbleibende Molekül umstellt. Dies geschieht beispielsweise, wenn das \(HCO_3^-\) aus dem Blut in der Lunge zu \(CO_2\) und \(OH^-\) ragiert, woraufhin wir das \(CO_2\) ausatmen. Siehst du, wie hier Veränderungen im zurückbleibenden Teilchen die Abspaltung des \(OH^-\) begünstigen?
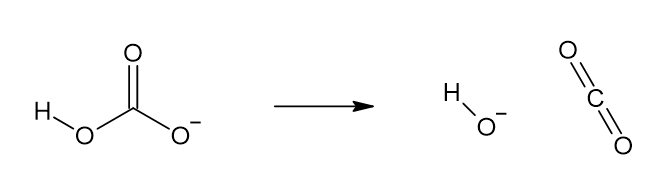
Abb 3: Abspaltung von Hydroxid-Ionen aus Hydrogencarbonat-Ionen.¶
Weiter zur nächsten Seite
Zurück zum Start
Zurück zum Molekularium